Carcinoma hepatocelular: diagnostico, estadificación y estrategia terapéutica.
COMENTARIO
En el siguiente articulo por estudios completos comparativos, se da desde el año 2000 con bases bien establecidas diagnósticos que antes eran solamente descritos y aceptados por anatomo-patologia, lo cual demuestra la pericia y alta especificidad y sensibilidad, en manos expertas de los radiólogos el buen uso de esta herramienta. Se recomienda nuevamente reforzar y practicar constantemente el uso de los diversos equipos y de acuerdo a las necesidades de cada estudio optimizar los recursos
Servicio de Radiodiagnóstico, Centro de Diagnóstico por imagen (CDIC), Hospital Clinic Barcelona España . Unidad de Oncologia Hepática (BCLC group), CIBERend, IDIBAPS, Universidad de Barcelona, Barcelona, España.
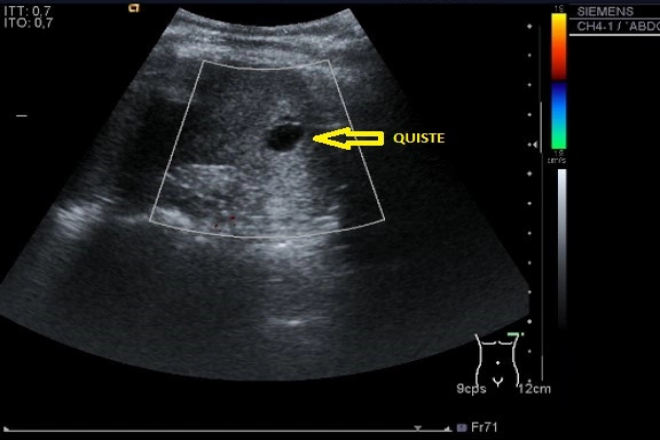
El carcinoma hepatocelular es un tumor de elevada incidencia y alta mortalidad; estos datos justifican los programas de detección precoz para poder aplicar los tratamientos considerados curativos, lo que implicará una mayor supervivencia. La detección precoz debe realizarse mediante ecografía semestral en la población con riesgo de padecer este tipo de tumor, fundamentalmente en pacientes con cirrosis hepática. Debido a sus características vasculares, actualmente se puede realizar el diagnostico de carcinoma hepatocelular por técnicas de imagen dinámicas (ecografía con contraste/TC/RM). En caso que el patrón de captación no sea característico en estas técnicas de imagen debe efectuarse una biopsia de la lesión.
La prevención eficaz de la muerte de carcinoma hepatocelular es evitando la adquisición de factores de riesgo, un buen ejemplo fue la caída drástica de la incidencia de CHC en Taiwan por la aplicación universal de vacuna frente a VHB; lamentablemente una vez que se ha desarrollado la cirrosis hepática el riesgo de CHC se mantiene a pesar de obtener una respuesta viral persistente tras tratamiento y el único método eficaz para poder disminuir la mortalidad asociada Al CHC es diagnosticar la enfermedad de forma precoz por programas específicos.
SEGIMIENTO PARA LA DETECCION PRECOZ DE CHC
Para la estrategia sea efectiva y pueda impactar en la supervivencia de los pacientes se debe definir la población de riesgo a la que debe ir dirigido el estudio
1.- Población de riesgo: pacientes con cirrosis hepática de cualquier etiología (vírica, abuso de alcohol, hemocromatosis, autoinmune, etc.) cuyo estado general permita tratamiento en caso de encontrar una lesión focal hepática maligna. En los pacientes afectos de una cirrosis evolucionada descompensada ( estadio CHILD-PLUGH C) solo se seguirá a los que sean candidatos a trasplante.
2.- Técnicas de Cribado: para la detección precoz en fase asintomática del CHC de bajo coste, sensibilidad aceptable, fácil aplicación, repetible, disponible y sin riesgos asociados. Se dividen en serológicos (marcadores tumorales) técnicas de imagen ( USG, TC, RM) .
La ecografía es la técnica menos invasiva, se puede repetir sin ningún riesgo para el paciente, sensibilidad elevada (60-80%) y especificidad (45-96%) en el dxco de CHC, con el uso de buenos equipos y del personal adecuadamente capacitado.
Por lo tanto la ecografía es la técnica de cribado de elección, en alteraciones difusas del parénquima hepático será fácilmente detectable un nódulo bien definido, diferente del resto del parénquima, mientras que en el hígado muy nodular existirán tantas imágenes correspondientes a nódulos de regeneración que un nuevo nódulo puede pasar desapercibido.
El CHC en fase inicial suele ser único, si bien en cerca del 20% de los casos puede ser multinodular por la aparición simultánea de varios focos de tumor. Los tumores pequeños son predominantemente hipoecoicos, pero la presencia de grasa hace que sean hiperecogénicos en algunos casos; el diagnóstico diferencial de los pequeños nódulos detectados durante el seguimiento deberá establecerse con lesiones benignas: angiomas, hamartomas, nódulos de regeneración y displasia de bajo grado. Las lesiones malignas que pueden hallarse en un paciente con cirrosis hepática son en, primer lugar el CHC, pero también podemos encontrar metástasis y colangiocarcinomas periféricos (CCP). La aparición de linfomas B asociados a los virus B y C son infrecuentes, pero el hecho de ser múltiples lesiones hipoecoicas de pequeño tamaño los puede diferenciar de las otras entidades.
Los tumores de gran tamaño suelen ser heterogéneos ya que presentan tabiques en el interior y zonas con diferente grado de necrosis, vascularización y fibrosis. Pueden persistir como una lesión única encapsulada , en fases más avanzadas existirán múltiples lesiones de límites más o menos precisos y con invasión vascular. El CHC tiene tendencia a invadir las venas hepáticas y/o porta, produciendo un aumento de tamaño del vaso cuyo aspecto es sólido, con vascularización arterial en su interior.
3.- intervalo de las pruebas: el tiempo de duplicación del CHC no está bien establecido, aunque algunos estudios indican que está alrededor de los 2–4 meses; exploraciones cada 3 meses comportan la observación de más imágenes nodulares comparado con los estudios cada 6 meses pero no incrementan el diagnóstico precoz ya que lo que se detecta son más nódulos benigno EN RESUMEN
Las sociedades científicas han aceptado que el intervalo recomendado debe ser de 6 meses
En resumen, las recomendaciones de los expertos son:
- El seguimiento de los pacientes con riesgo de padecer un CHC debe efectuarse mediante ecografía cada 6 meses.
- No debe emplearse la AFP para el cribado
Diagnóstico de CHC
Antes del año 2000, la confirmación diagnóstica del CHC debía realizarse mediante su estudio anatomopatológico; los riesgos las limitaciones de la punción biopsia hepática con aguja fina (PBHAF) llevaron a la búsqueda de otros métodos diagnósticos alternativos.
Las conclusiones de la conferencia monotemática de la EASL (European Association for the Study of the Liver) sobre el manejo del CHC celebrada en Barcelona en el año 2000 definieron por vez primera unos criterios de diagnóstico no invasivo que permitían establecer un diagnóstico definitivo de CHC en pacientes cirróticos sin necesidad de confirmación citohistológica en los nódulos mayores de 2 cm 34. En el año 2005 se revisaron los criterios de diagnóstico no invasivo por parte de la AASLD (American Association for the Study of Liver Diseases); dichos criterios se publicaron en las guías de práctica clínica del CHC8 y han sido aceptados por la EASL y por un grupo de expertos de las diferentes sociedades científicas nacionales implicadas en el manejo del CHC9. Estos criterios se basan en la detección del patrón vascular característico definido por captación homogénea del contraste en fase arterial seguido de lavado de contraste en fase venosa.
Con el fin de optimizar la estrategia diagnóstica, las guías de práctica clínica propuestas por la AASLD sugieren un algoritmo diagnóstico, que se basa en la realización de técnicas de imagen dinámicas (US con contraste, TC multifásica, RM dinámica). La secuencia de las pruebas viene determinada por el tamaño del nódulo a estudiar:
- 1. Lesión > de 2cm de diámetro: se puede establecer el diagnóstico concluyente de CHC si alguna de las técnicas de imagen descritas muestra el patrón vascular característico de CHC ; En caso contrario se recomienda la obtención de una biopsia.
CHC de 30mm en LHD con un patrón vascular característico. Estudio RM dinámico. A) Fase arterial, la lesión se realza intensamente en relación al hígado de vecindad. B) Fase portal, el nódulo lava su contraste más rápidamente que el hígado circundante. CHC de 30mm en LHD con un patrón vascular característico. Estudio RM dinámico fase arterial, la lesión se realza intensamente en relación al hígado de vecindad; fase portal, el nódulo lava su contraste más rápidamente que el hígado circundante.
- 2. Lesión de 1–2cm de diámetro: con la finalidad de evitar lecturas controvertidas, se exige la demostración del patrón vascular característico de forma coincidente mediante 2 técnicas de imagen; en caso contrario, debe realizarse una biopsia.
Nódulo subcapsular de CHC de 16mm En LHD con patrón vascular típico coincidente en dos técnicas de imagen.
Figura 4. Nódulo subcapsular de CHC de 16mm En LHD con patrón vascular típico coincidente en dos técnicas de imagen
- 3. Lesiones <de 1cm: en la mayoría de los casos son lesiones benignas que no crecen o bien desaparecen durante el seguimiento. Además, su correcta caracterización mediante técnicas de imagen o biopsia es en muchas ocasiones imposible. Por tanto, ante la detección de un nódulo infracentrimétrico se recomienda un control estrecho mediante ecografía con un intervalo de 3–4 meses. Si la lesión permanece estable al cabo de 18–24 meses, se puede volver al seguimiento estándar cada 6 meses mediante US. En caso de crecimiento, se actuará de acuerdo al tamaño que haya alcanzado el tumor.
Es interesante destacar que un pequeño porcentaje de nódulos de CHC de tamaño inferior a 20mm son hipovasculares en la fase arterial de los estudios dinámicos de imagen, probablemente por el desarrollo insuficiente de una red arterial de vasos neoformados;por ello, con los criterios de diagnóstico no invasivos, únicamente se podrán diagnosticar aquellos CHC que hayan desarrollado una completa neoangiogénesis, hecho que en muchas ocasiones no ocurre en lesiones por debajo de 2cm de tamaño. Por tanto, la biopsia tiene un rol importante en el diagnóstico precoz del CHC.
La biopsia de los nódulos hepáticos se hace habitualmente bajo control ecográfico. La punción puede realizarse indistintamente con aguja de aspiración (PAAF) o con aguja de corte
En los últimos años han aparecido avances en el uso de técnicas de imagen para el diagnóstico del CHC. En este sentido, la RM empleando contrastes órgano específicos como son los SPIO, captados por las células de Kuppfer, y los contrastes hepatobiliares, captados por los hepatocitos, han demostrado un rendimiento diagnóstico similar a la TC multidetector .
Otro avance importante en el campo del diagnóstico por imagen del CHC ha sido el desarrollo de la ecografía con contraste. Esta técnica permite caracterizar las lesiones nodulares detectadas mediante ecografía y constituye un complemento ideal para confirmar los hallazgos obtenidos mediante RM/TC.
Deben realizarse algunas consideraciones,en primer lugar, debe tenerse en cuenta que los contrastes ecográficos que actualmente se utilizan son puramente intravasculares, a diferencia de los contrastes empleados en la TC y RM que pueden pasar al espacio intersticial; esto puede condicionar resultados discordantes de algunas lesiones hepáticas estudiadas mediante Ecografía con contraste o la TC/RM; puede ser útil exponer algunos aspectos de los patrones de captación de lesiones que podemos encontrar en el seguimiento de un paciente cirrótico.
Los nódulos de regeneración, las displasias de bajo grado y los hamartomas no presentan captación arterial. Los angiomas presentan captación arterial periférica que posteriormente se hace iso-hipercaptante y homogénea en fases tardías, siendo el patrón característico. Los angiomas de pequeño tamaño pueden presentar infrecuentemente, captación arterial completa, permaneciendo iso-hipercaptantes con respecto al parénquima en fases tardías.
La displasia de alto grado suele presentar hipercaptación arterial, manteniéndose isocaptante en fases portales y tardías, ya que a diferencia del CHC, conservan la vascularización portal; metástasis hepáticas suelen presentar una captación arterial, habitualmente anular, seguida de un aclaramiento rápido del contraste en fases venosas, indicativas de malignidad.
En ocasiones, en el mismo paciente se detecta de forma simultánea una lesión benigna y una maligna. En esos casos, las técnicas de imagen dinámicas nos pueden ayudar a diferenciarlas y precisar cuál es la lesión diana de posibles biopsias diagnósticas o tratamientos percutáneos.
Artículo escrito por el Dr Juan Luis González Díaz