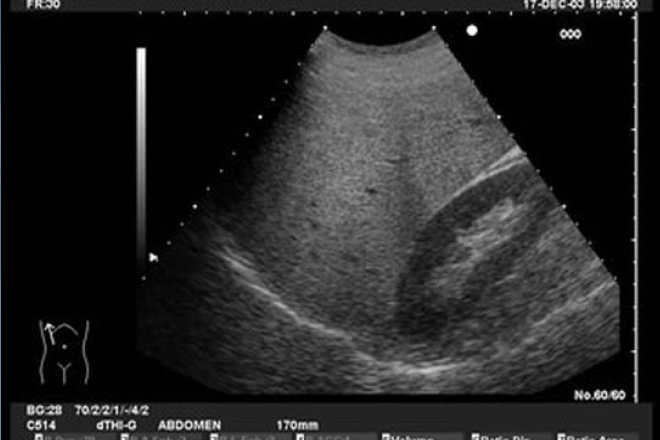
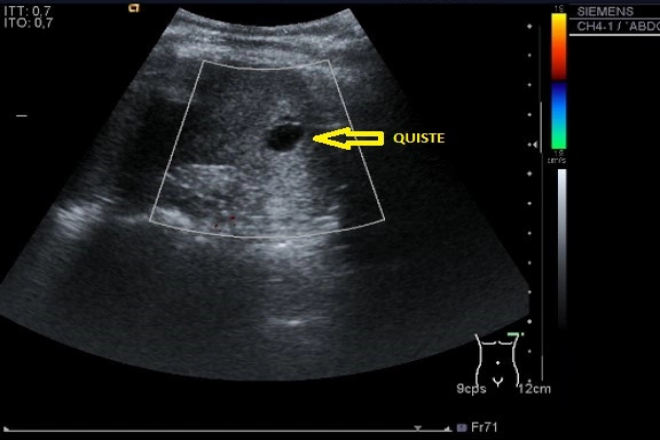
Hígado graso no alcohólico
A la luz de la evidencia actual,
se afirma que los AGL pueden causar toxicidad directamente por el incremento
del estrés oxidativo y por la activación de las vías inflamatorias, mediante la
inducción de algunos citocromos p-450 y de lipoxigenasas microsomales que
producen especies radicales de oxígeno (ERO), en el contexto de un defecto en
la fosforilación oxidativa mitocondrial que puede resultar en un incremento de
las ya mencionadas especies reactivas de oxígeno. Sin embargo, parece ser
que la acumulación de los triglicéridos hepáticos, lejos de lo que se presume,
podría ser un mecanismo protector que previene el efecto tóxico de los AGL no
esterificados.
Adicionalmente se ha propuesto un nuevo componente en la génesis de este
fenómeno: el llamado “tercer golpe”, que es la inadecuada proliferación
hepatocitaria. En el hígado sano la muerte celular estimula la replicación de
los hepatocitos maduros que reemplazan las células muertas y reconstituyen la
función del tejido normal. Sin embargo, el estrés oxidativo, característica
central en la patogenia del HGNA, inhibe la replicación de los hepatocitos
maduros llevando a una expansión de la población de células progenitoras
hepáticas.
Estas células pueden
diferenciarse tanto en células ovales como en células intermedias, semejantes a
los hepatocitos, que están fuertemente correlacionadas con el estado de
fibrosis. En el daño mantenido el desarrollo de fibrosis/cirrosis es
dependiente de la eficacia de los hepatocitos en regenerarse. Por lo tanto, la
muerte celular con una proliferación alterada de los hepatocitos progenitores
representa el mencionado “tercer golpe”.
El papel del estrés oxidativo y la disfunción mitocondrial en la EHNA se
encuentra bien establecido, y su relación con el avance de la enfermedad es
directamente proporcional. La β-oxidación dentro del hígado se efectúa en la
mitocondria, pero en el contexto del HGNA, este proceso se acelera debido al
incremento de los ácidos grasos (sustratos), lo que genera un aumento de las
especies reactivas de oxígeno que inducen el estrés oxidativo, llevando a la
activación de las vías inflamatorias y también al daño mitocondrial.
Otros mecanismos implicados en la patogenia de la EHNA incluyen al estrés del
retículo endoplásmico, la endotoxemia derivada del intestino y los
glucocorticoides. El estrés del retículo endoplásmico se produce por otros
estreses biológicos como la hiperinsulinemia y la hiperlipemia, llevando a la
activación de varias vías que, a su vez, llevan a la insulinorresistencia, la
inflamación, la apoptosis y la disfunción mitocondrial.
La endotoxemia se produce por un sobrecrecimiento bacteriano y aumento de la
permeabilidad del intestino delgado. Éste, a su vez, lleva a la producción de
etanol y a la liberación de lipopolisacáridos, los que activan la producción de
TNF-α por las células de Kupffer, induciendo la inflamación hepática.
Los glucocorticoides de origen exógeno y endógeno son fuentes bien reconocidas
de HGNA. Los pacientes con síndrome de Cushing, que tienen niveles altos de
glucocorticoides, desarrollan un fenotipo metabólico característico de obesidad
central.
El mecanismo por el cual esto promueve la acumulación de grasa hepática incluye la inhibición de la β-oxidación y la promoción de la lipólisis de novo del hígado. Sin embargo, la mayoría de los pacientes con HGNA tienen niveles normales de cortisol en plasma, lo que sugiere que los mecanismos específicos a nivel tisular son los que dirigen tal disfunción metabólica.
Estos hallazgos llevaron a un creciente interés en dos vías enzimáticas que juegan un papel clave en el metabolismo local de los glucocorticoides y la consecuente disponibilidad de éstos para unirse y activar el receptor de glucocorticoides: la 11β-hidroxiesteroide deshidrogenasa tipo 1 (11β-HSD1) y las enzimas reductasas del anillo A (5-α- y 5-β). La primera de ellas convierte la cortisona inactiva en cortisol activo. Su inhibición disminuye el peso corporal y el perfil lipídico, y mejora la tolerancia a la glucosa. La segunda vía, por su parte, es la responsable del metabolismo del cortisol inactivándolo a tetrahidrometabolitos. En modelos animales en los que se ha inhibido la actividad de dichas enzimas se ha desarrollado insulinorresistencia e hígado graso, por lo se convierten en potenciales sitios de intervención terapéutica para prevenir el desarrollo y la progresión del HGNA.
Artículo escrito por la Dra. Martha Alejandra Eusebio Hernández