SÍNDROME DE OVARIO POLIQUÍSTICO. DIAGNÓSTICO Y MANEJO
El síndrome de ovario poliquístico (SOP) es un trastorno endocrino metabólico altamente prevalente.
Debe sospecharse en mujeres con hirsutismo u otras manifestaciones cutáneas de hiperandrogenismo, irregularidades menstruales y obesidad.
El síndrome de ovario poliquístico es un diagnóstico de exclusión. El diagnóstico oportuno es importante ya que este síndrome se asocia a riesgos reproductivos, oncológicos y metabólicos.
El tratamiento debe iniciarse siempre con la corrección de las alteraciones metabólicas.
INTRODUCCION
Es la causa más común de hiperandrogenismo con una incidencia de un 3% tanto en mujeres adolescentes como adultas.
Está presente en el 75% de las mujeres hirsutas y en el 10% de las mujeres premenopaúsicas.
Su etiología es incierta y se manifiesta por síntomas y signos variados que afectan a cada mujer en forma particular. Destacan las irregularidades menstruales, las manifestaciones cutáneas del hiperandrogenismo, la obesidad, la infertilidad, la resistencia insulínica (RI) y el aspecto poli- quístico de los ovarios en la ultrasonografía.
RI juega un papel preponderante en las consecuencias metabólicas a largo plazo del síndrome, entre las que cabe destacar la diabetes tipo 2, la enfermedad cardiovascular y el hígado graso no alcohólico.
DEFINICIÓN
SOP puede ser diagnosticado en pacientes que presentaran a lo menos dos de las tres características siguientes: hiperandrogenismo clínico o bioquímico, oligo-ovulación, y presencia de ovarios de morfología poliquística, dando origen a cuatro fenotipos.
Fenotipos A y B cumplen con los criterios NIH y son considerados formas
Clásicas, C y D están en discusión.
Los ovarios poliquísticos no necesariamente deben estar presentes para definir la enfermedad y la presencia de ovarios poliquísticos por sí solo no establecen el diagnóstico.
En adolescentes se ha planteado que el diagnóstico debería basarse en el hiperandrogenismo bioquímico asociado a irregularidades menstruales y morfología de ovarios poliquísticos.
FISIOPATOLOGÍA
Destacan al menos tres tipos de alteraciones interrelacionadas entre sí: una disfunción neuroendocrina (hipersecreción de LH), un trastorno metabólico (resistencia insulínica e hiperinsulinemia) y una disfunción de la esteroidogénesis y de la foliculogénesis ovárica.
Disfunción neuroendocrina
Caracterizada por aumento de la secreción de LH y una secreción de FSH normal o disminuida.
Disfunción metabólica.
RI periférica que se expresa por una hipersecreción de insulina.
Dando mayor secreción de andrógenos por el ovario y las suprarrenales; estimula la secreción de LH y además disminuye la síntesis hepática de la SHBG.
Se asocia fundamentalmente a los fenotipos clásicos que cursan con hiperandrogenemia.
En el síndrome de ovario poliquístico semejante a lo descrito en la diabetes 2, la RI precede a la disminución de la tolerancia a la glucosa. No todas las pacientes con SOP y RI de- sarrollan una intolerancia a la glucosa y una diabetes tipo 2, por lo que se ha sugerido que en estos casos, debe coexistir una disfunción de la célula β-pancreática la cual podría ser condicionada por el mismo defecto que genera la resistencia insulínica o por otros factores.
disfunción de la esteroidogénesis ovárica/suprarrenal.
Es un pilar fundamental en este síndrome y se caracteriza por una alteración de la biosíntesis de los andrógenos, la cual tanto en el ovario como en la suprarrenal está determinada por la actividad de una enzima denominada citocromo P450c17.
El hiperandrogenismo adrenal funcional está presente en alrededor del 50% de las mujeres con síndrome de ovario poliquístico, y se expresa por una elevación moderada de DHEAS.
El tejido adiposo juega un papel preponderante en la fisiopatología del SOP ya que tiene una función esteroidogénica intrínseca y es un tejido blanco para los andrógenos.
disfunción de la foliculogénesis.
SOP presentan un pool de folículos en crecimiento 2 a 3 veces superior que las mujeres sanas.
Hay un aumento de folículos preantrales y antrales pequeños y un mayor reclutamiento folicular.
Detención del proceso de selección folicular, lo que explica la ausencia de ovulación.
ETIOPATOGENIA
Factores ambientales destacan la obesidad y los eventos que ocurren en la vida intrauterina (hiperandro- genismo, diabetes gestacional y sobrepeso de la madre durante el embarazo)
MANIFESTACIONES CLÍNICAS
El cuadro clínico es muy polimorfo y varía de acuerdo a la edad de la paciente.
Inician en el período perimenárquico con la aparición de alteraciones menstruales en los dos tercios de las adolescentes principalmente oligomenorrea, alternados con períodos de amenorrea secundaria.
Adrenarquia prematura o una pubertad precoz pueden ser el debut del cuadro clínico.
El hirsutismo por lo general es discreto o moderado , se presenta en dos tercios de las pacientes, aparece después de la pubertad y progresa lentamente o se detiene alcanzada la madurez sexual.
La virilización es rara y su presencia debe hacer sospechar otras etiologías como un tumor secretor de andrógenos o una hiperplasia adrenal congénita.
La obesidad está presente en alrededor de la mitad de las pacientes y es típicamente de tipo androide o “forma de manzana”, inicia en la niñez y se acentúa en la pubertad.
En las pacientes obesas y/o hiperinsulinémicas puede observarse acantosis nigricans que es un marcador cutáneo de resistencia insulínica.
EXAMEN FÍSICO
Para consignar la distribución del vello y su cuantificación se utiliza el score de Ferriman-Gallwey.
Clásicamente en mujeres en edad reproductiva se considera que un cómputo superior a 8 indicaría hirsutismo.
Es aconsejable completar el examen físico con la medición de la presión arterial, el examen del tiroides y de las mamas y la inspección de los genitales externos en busca de clitoromegalia en las niñas y un examen ginecológico en las mujeres sexualmente activas.
Recordar que el cuadro clínico es polimorfo. No todas las mujeres presentan la totalidad de los síntomas. Sin embargo es importante conocerlos ya que pueden ser la pista que lleven a un diagnóstico oportuno.
LABORATORIALES
tienen andrógenos elevados en forma discreta o moderada ya sea testosterona, andros- tenediona, dehidroepiandrosterona sulfato, o todos ellos.
testosterona total. Es el andrógeno circulante más importante en la mujer y es también el principal andrógeno causante de hirsutismo.
En el SOP la testosterona total sólo está elevada discretamente en el 50% de los casos.
Para establecer la presencia de hiperandrogenismo, el consenso de Rotterdam sugiere uti- lizar el índice de andrógenos libres (IAL).
Consiste en la relación entre la testosterona total y su proteína transportadora (SHBG) de acuerdo a la siguiente fórmula: Testosterona (nmol)/ SHBG (nmol)x 100 (Valor normal < 4.5). Para transformar la T en ng/ml a nmol/l debe multiplicarse el valor x 3.467.
dehidroepiandrosterona sulfato (dHEAS).
Se la utiliza como marcador de hiperandrogenismo suprarrenal.
Androstenediona.
Es un andrógeno fundamentalmente de origen ovárico y puede ser el único andrógeno elevado en una mujer con SOP.
17 hidroxiprogesterona (17-oHP).
Es el mejor metabolito para des- cartar déficit de la enzima 21-hidroxilasa; su valor normal en ayunas en fase folicular temprana del ciclo menstrual es inferior a 2 ng/ml. Valores superiores a 6 son indicadores de bloqueo enzimático.
Relación LH/fSH.
Las pacientes con síndrome de ovario poliquístico frecuentemente (60%) tienen una relación LH/FSH aumentada.
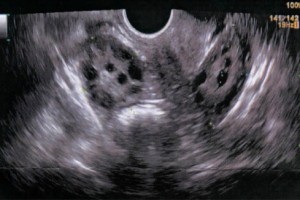
ULTRASONOGRAFÍA
La ultrasonografía especialmente transvaginal es un procedimiento útil para detectar morfología de ovarios poliquísticos. Se debe tener en cuenta que la vía abdominal tiene limitaciones sobretodo en niñitas obesas.
En pacientes portadoras de SOP el volumen es significativamente mayor, superiores a 10cc. No obstante, un 30% de las pacientes pueden presentar volúmenes ováricos normales.
Criterios actualmente utilizados para definir ovarios poliquísticos son: presencia de 12 o más folículos en cada ovario (barrido completo) que midan entre 2-9 mm de diámetro y/o un volumen ovárico aumentado (> 10 ml) en fase folicular temprana.
Sólo un ovario afectado es suficiente para definir el síndrome.
El estroma ovárico no está considerado en la definición ecográfica ac- tual de SOP. No obstante, cabe destacar que hasta un 94% de los casos de SOP presentan aumento de la ecogenicidad ovárica.
Enfoque diagnóstico.
El diagnóstico del síndrome de ovario poliquístico se basa en la combinación de sus características clínicas, bioquímicas y ultrasonográficas.
El diagnóstico diferencial del síndrome de ovario poliquístico debe es- tablecerse con otros cuadros clínicos que suelen presentar la asociación de hirsutismo y trastornos menstruales como: hiperplasia adrenal con- génita, tumores virilizantes, hiperprolactinemia, síndrome de Cushing, acromegalia y el uso de drogas como esteroides anabólicos y ácido valproico.
TRATAMIENTO
En la mujer que no desea embarazo, el tratamiento está orientado a corregir la hiperandrogenemia, las manifestaciones cutáneas del hipe- randrogenismo (hirsutismo, acné y alopecía androgénica), los trastornos menstruales y las alteraciones metabólicas asociadas a la resistencia insulínica y al hiperinsulinismo.
Los métodos que se pueden utilizar para un adecuado manejo del hiperandrogenismo están dirigidos a: inhibir la esteroidogénesis ovárica, suprarrenal o ambas, aumentar la concentración de SHbG, evitar la acción de andrógenos en tejidos blancos, bloqueando la unión a sus receptores e inhibir la conversión periférica (5-α re- ductasa) de testosterona a dihidrotestosterona (hormona 3 veces más potente) y por último, actuar directamente sobre los tegu- mentos, utilizando recursos cosméticos.
Los anticonceptivos orales. Son considerados la primera alterna- tiva terapéutica para mujeres en edad reproductiva, estos fármacos suprimen la secreción de LH y, por lo tanto disminuyen la biosínte- sis de andrógenos ováricos, aumentan la concentración plasmática de SHBG disminuyendo los andrógenos libres y además permite una descamación regular del endometrio, pero pueden deteriorar la resistencia insulínica y aumentar la síntesis hepática de triglicéridos.
Progestinas más recomendables son, la drosperinona, al ser un derivado de la espironolactona, tendría un efecto beneficioso sobre la resistencia insulínica y el dienogest y acetato de clormadino- na tendrían la capacidad de reducir la actividad de la 5 alfa reductasa a nivel de la piel.
Los antiandrógenos. Son compuestos de tipo esteroidal, como el acetato de ciproterona y la espironolactona, o no esteroidal, como la flutamida y el finasteride, que antagonizan al receptor de andrógenos en el folículo piloso y la glándula sebácea.
Inducción de ovulación. Consiste en el tratamiento farmacológico o quirúrgico destinado a inducir ciclos ovulatorios normales (mono foliculares) en pacientes con oligo-anovulación. Estos procedimientos son de resorte del especialista en medicina reproductiva.
Dándonos
Me pareció interesante dicho artículo ya que nos da una guía clínica muy práctica acerca de cómo abordar a la paciente con ovario poliquístico además de un panorama muy amplio de dicha patología englobando fisiopatología así como manifestaciones clínicas.
Y como pocos incluye la descripción ultrasonografíca de dicha patología.